来源:澎湃新闻 2025年3月17日
标题:CCS Chemistry | 上海师范大学赵宝国:吡哆醛催化自由基羰基过程实现苄胺与大位阻烷基碘…
作者:CCS Chemistry
CCS Chemistry是由中国化学会创办的高水平旗舰新刊,面向全球科学家,收录化学各领域高质量原创科技论文。关注CCS Chemistry,即时获取期刊相关资讯。
近日,上海师范大学赵宝国团队报道了吡哆醛催化苄胺与大位阻烷基碘代物的直接α-C-H交叉偶联反应,得到一系列大位阻α-支链苄胺/环胺。该反应通过单电子氧化(SET)途径,首次实现了自由基羰基催化过程。
背景介绍:
α-氨基自由基是一类具有高活性和合成价值的片段,可参与C-C键形成和π-键加成,具有广泛的合成应用潜力 (图1a)。然而α-氨基自由基的不稳定性和短暂的寿命限制了它在合成中的应用。为了解决这个问题,化学家们通过引入适当的醛或酮保护基,形成共轭作用稳定的2-氮杂烯丙基自由基,进而调控相关的反应。在该领域,Walsh及其同事以做出了开创性的研究,他们发现二苯甲酮-苄胺亚胺负离子能够与卤代烷发生单电子转移,生成相对稳定的2-氮杂烯丙基自由基,该自由基与烷基自由基复合生成α-取代的苄胺产物(图1b)。我们设想:以醛或酮为羰基催化剂,催化产生相对稳定的2-氮杂烯丙基自由基,进一步与自由基物种或π-体系反应,实现伯胺的α-C-H直接官能化。尽管羰基催化能够有效促进伯胺α位与亲电试剂的直接反应,但自由基历程的羰基催化过程尚未建立。
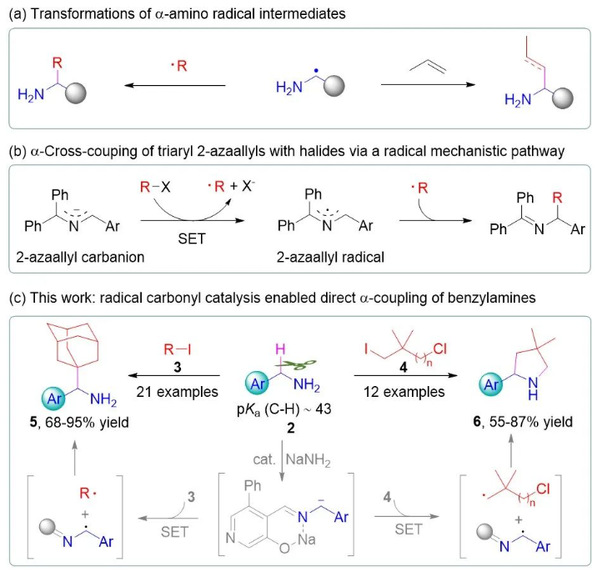
图1. 研究背景与本文工作
本文亮点:
基于上述研究背景,作者用吡哆醛为催化剂,成功实现了苄胺与大位阻烷基碘代物的直接α-C-H交叉偶联,以68-95%的收率获得了各种位阻庞大的α-支链苄胺。对于末端含有氯的碘代物,可以继续发生分子内环化,得到各种环胺化合物 (图1c)。作者以间苯基苄胺与1-金刚烷碘为模板底物,进行了一系列条件优化,并在最优反应条件下,对苄胺和烷基碘的底物范围进行了考察(图2和3),该反应具有良好的底物适用性和官能团兼容性。药物和天然产物中的结构,如吉非罗齐 (5s)、美研醇 (5t)和氢化松香 (5u和5v)等衍生物均可以成功地整合到苄胺的α位。此外,作者对该反应进行了克级规模实验,产率并未降低。
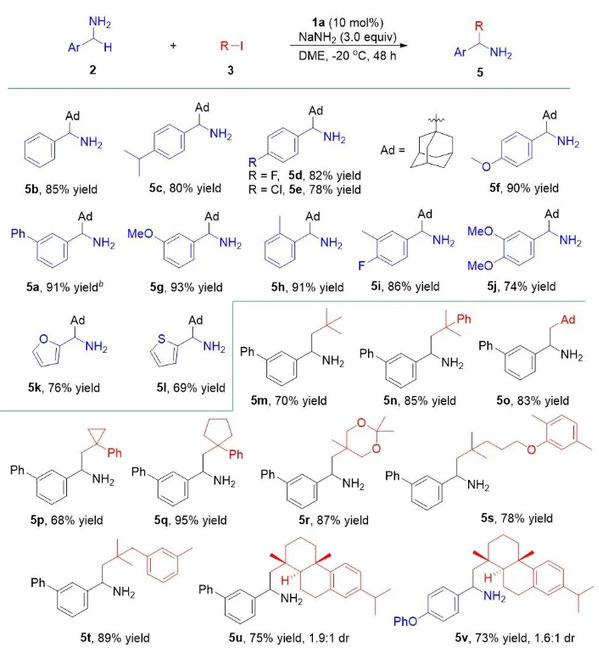
图2. 苄胺以及烷基碘底物拓展
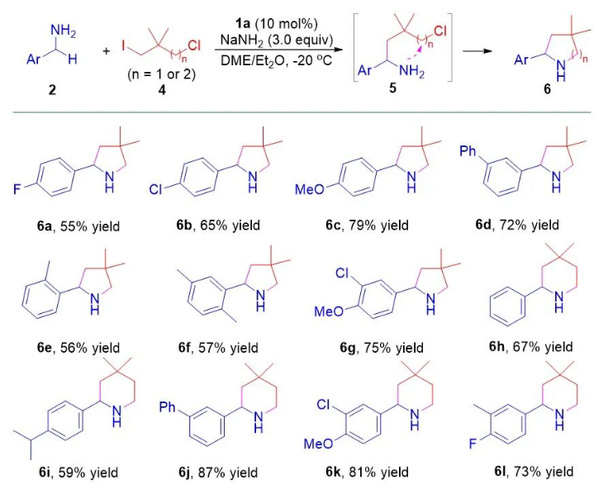
图3. 交叉偶联/环化的底物拓展
为了研究反应机理,作者进行了自由基钟实验,实验结果表明该反应经历了自由基过程 (图4)。据此,作者提出了可能的反应机理 (图5):在NaNH2存在下,苄胺2与吡哆醛催化剂1a缩合形成亚胺钠盐13。随后被NaNH2拔去质子形成离域的α-氨基碳负离子14,它与烷基碘3发生单电子转移 (SET),生成2-氮杂烯丙基自由基15和烷基自由基16。自由基交叉偶联得到中间体17。17与苄胺2反应释放出产物5并再生亚胺钠盐13,完成催化循环。亚胺13的形成活化了苄基C-H键,并显著提高了其C-H酸度,高达1012倍,促进了13去质子化为碳负离子14。作者所提出的机理也得到了计算研究的支持 (图6)。
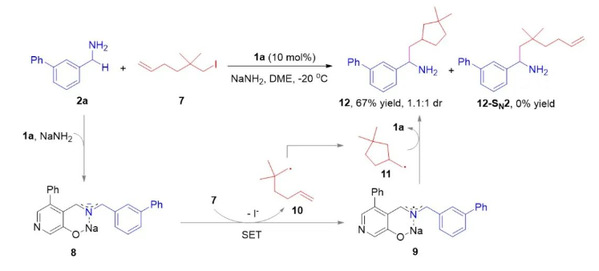
图4. 自由基钟实验
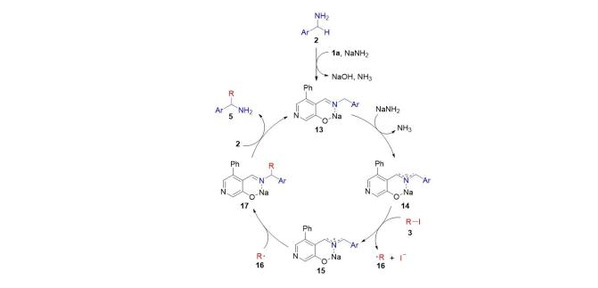
图5. 可能的反应机理
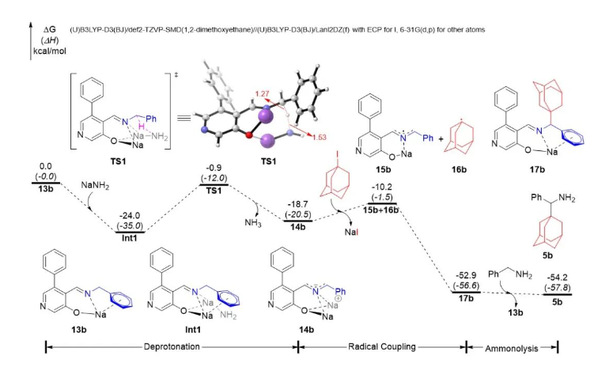
图6. DFT计算
最后,作者通过使用手性吡哆醛作为催化剂,还初步探索了不对称α-交叉偶联(图7)。虽然反应的对映选择性中等 (77% ee),但该结果展示了手性吡哆醛在不对称自由基羰基催化中的对映选择性诱导能力。
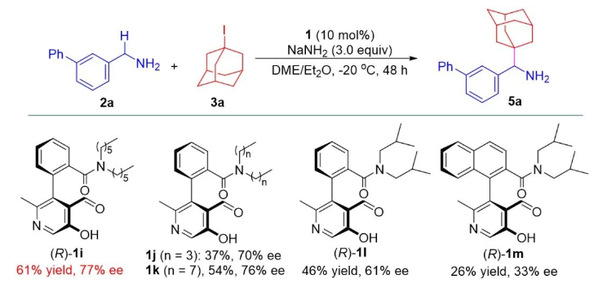
图7. 不对称烷基化的初步研究
总结与展望:
综上所述,使用吡哆醛作为催化剂,本文成功地实现了NH2未保护的苄胺2与大体积烷基碘3和4的直接α-交叉偶联反应。该反应为在苄胺的α位引入大位阻取代基提供了一种高效新策略。该反应经历了自由基羰基催化策略,为伯胺的直接α-C-H转化开辟了一条新途径。
该工作以Research Article的形式发表在CCS Chemistry。上海师范大学赵宝国教授与刘思琪老师为通讯作者,博士后侯承康为第一作者。特别感谢国家重点研发计划、国家自然科学基金和上海市科技重大专项等项目的资助。
文章详情:
Direct α-Cross-Coupling of Benzylamines with Bulky Alkyl Iodides Enabled by Radical Carbonyl Catalysis
Chengkang Hou, Longjie Huang, Lei Wang, Siqi Liu*, Guoqing Zhao, Kuiling Ding, Baoguo Zhao*
Cite This by DOI: 10.31635/ccschem.025.202405131
链接地址:https://m.thepaper.cn/baijiahao_30422025
